全国高考化学实验题解题策略初探
注:本文刊载于2016.4《推荐国内安全的网赌网站》(推荐全球最大网赌正规平台欢迎您主管)P33~35
全国高考化学实验题解题策略初探
张士碧
(推荐全球最大网赌正规平台欢迎您 福建漳平 364400)
摘要:研读全国高考考试大纲、考试说明,分析典型高考实验题,提出高考化学实验题解题策略:一、熟悉试题结构,优化审题过程;二、重视题给信息,主动迁移应用;三、熟练题型解法,训练规范作答。
关键词:高考实验题、审题、解题、信息
文章编号 中图分类号 文献标识码
《推荐全球最大网赌正规平台欢迎您》“考核目标与要求”对化学学习能力的要求有三点:1.接受、吸收、整合化学信息的能力;2.分析和解决(解答)化学问题的能力;3.化学实验与探究能力[1];《推荐全球最大网赌正规平台欢迎您》“考试范围和内容”中“化学实验”共有7条,其中核心内容(6)“能根据要求,做到①设计、评价或改进实验方案;②了解控制实验条件的方法;③分析或处理实验数据,得出合理结论;④识别典型的实验仪器装置图” [2],高考实验综合题很好地体现了考试大纲和考试说明对化学学习能力的考查要求。认真钻研全国考试大纲和考试说明,分析近年高考实验综合题,探索高考试题的命题规律,笔者提出高考实验题的解题策略,举例分析如下。
一、熟悉试题结构,优化审题过程
高考实验试题结构一般分题头、流程图、问题三部分。题头一般简要介绍实验目的(制备、提纯、测定等),流程图部分含实验需要的仪器装置图、物质性质和实验相关文字图表信息等,问题主要是依据实验中涉及的反应原理、仪器操作、实验误差、有关计算、实验方案等进行设置。
审题时先浏览全题,按照“实验目的→实验原理→实验流程→实验问题”顺序展开解题思路,能迅速把握试题的主旨,顺利解题。解题过程中,熟悉常见的实验装置顺序显得格外重要,例如对于常见制备实验,依据气流方向,一般的流程(装置连接顺序)是:造气→洗气(除杂、干燥)→主反应→收集→末装置(尾气处理、保护装置)。
熟悉试题结构,优化审题过程,审题能力和解题能力就会有较大提升。
例1(2011年全国高考卷28题)
氢化钙固体是登山运动员常用的能源提供剂。某兴趣小组拟选用如下装置制备氢化钙。
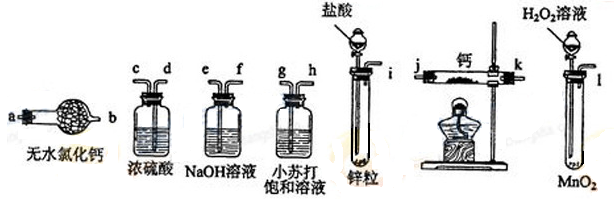
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为________(填仪器接口的字母编号)。
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞_________(请按正确的顺序填入下列步骤的标号)。
A.加热反应一段时间 B.收集气体并检验其纯度
C.关闭分液漏斗活塞 D.停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此判断,上述实验确有CaH2生成。
①写出CaH2与水反应的化学方程式 ___________________。
②该同学的判断不正确,原因是_________________。
(4)请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象___________。
(5)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是____________。
分析:此试题结构明显分题头、流程图、问题三部分,浏览全题后可按照“实验目的→实验原理→实验流程→实验问题”顺序展开解题。
(1)由H2气体流向得出实验流程为:造气→除HCl→干燥→主反应→保护装置,得出顺序为:i→e,f→d,c→j,k(或k,j)→a,可见熟悉制备实验装置顺序就能迅速解题。
(2)从实验目的和实验原理出发对实验操作进行分析,由实验安全性(防氢气与装置中空气混合加热爆炸)和对产品的保护(防空气中水蒸气、氧气等进入与CaH2反应)来回答。实验操作常会从实验安全方面考查。
(3)(4)均可由实验原理、物质性质进行实验方案评价和实验方案设计。
(5)可由安全性、可行性进行实验方案评价。
可见,实验题所设置的问题一般是从实验目的出发,依据实验过程涉及的原理、操作、流程、实验方案等设置。
审题时对试题结构和设问形式了然于胸,解题时才能有条不紊,迅速破题。
二、重视题给信息,主动迁移应用
高考实验题,特别是有机实验题,往往采用最新的科技信息进行命题,信息新颖,设问巧妙,依据高中化学知识能够解答,试题有“起点高、落点低”的特点。
题给信息就是提示信息,因为不提供这些信息,就考生现有知识水平无法解答,可见接受、吸收、整合题给信息就是成功解题的金钥匙。解题时出现障碍,一般是审题过程中对相关信息重视不够,应重新认真阅读信息,挖掘题给的有用信息主动迁移应用,就能克服障碍顺利解题。
新信息的处理、加工、应用能力是突破高考化学实验题的一大关键。
例2(2014年全国新课标Ⅰ卷26题)
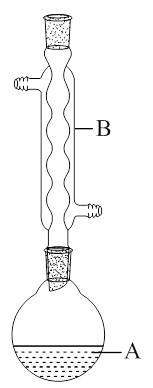
乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
 | |
实验步骤:
在A中加入4.4 g的异戊醇,6.0 g的乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A,回流50min,反应液冷至室温后倒入分液漏斗中,分别用少量水,饱和碳酸氢钠溶液和水洗涤,分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的名称是:__________________。
(2)在洗涤操作中,第一次水洗的主要目的是:________________;第二次水洗的主要目的是:________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
a. 直接将乙酸异戊酯从分液漏斗上口倒出
b. 直接将乙酸异戊酯从分液漏斗下口放出
c. 先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d. 先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口放出
(4)本实验中加入过量乙酸的目的是:________________________________。
(5)实验中加入少量无水MgSO4的目的是:________________________________。
(6)在蒸馏操作中,仪器选择及安装都正确的是:________________ (填标号)。
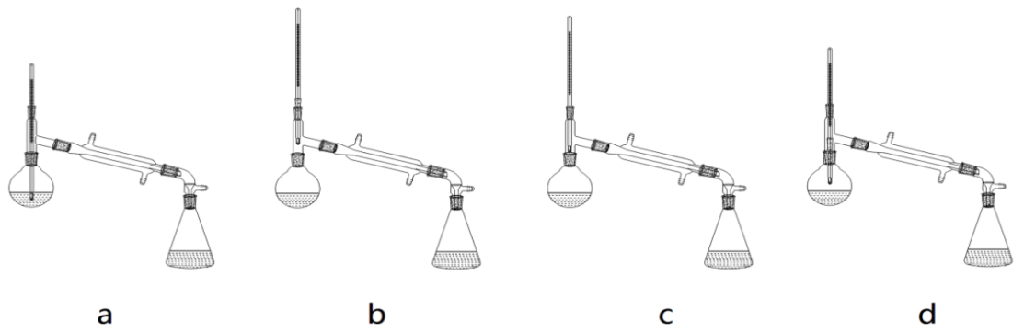
(7)本实验的产率是:________________(填标号)。
a. 30% b. 40% c. 50% d. 60%
(8)在进行蒸馏操作时,若从130℃便开始收集馏分,会使实验的产率偏______ (填“高”或“低”),其原因是________________________________。
分析:近年高考实验题连续使用有机新信息进行命题,其试题新颖,很好地考查学生接受、吸收、整合化学信息,分析和解决化学问题的能力,本题是信息丰富的有机实验题。
(1)球形冷凝管是有机实验常见仪器,其作用为冷凝回流。本小题考查仪器名称,属于实验基础内容的考查。
(2)对“水洗→盐洗(饱和碳酸氢钠溶液)→水洗”目的的考查,要根据实验操作过程信息和图表中各有机物水溶性信息,从除杂原理的角度来回答,可知第一次水洗洗掉大部分硫酸和醋酸,盐洗洗掉残余硫酸和醋酸,第二次水洗洗掉碳酸氢钠。
(3)答题关键是利用题给信息“乙酸异戊酯密度为0.8670g∙cm−3且难溶于水”,正确的分液操作选d。
(4)此问考查实验原理和化学平衡移动原理,利用题给化学方程式信息分析可知,加入过量乙酸的目的是提高异戊醇的转化率。
(5)只要重视题给信息“分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体”,不难得出加入少量无水MgSO4的目的是干燥。
(6)蒸馏操作装置的考查体现考试说明中“识别典型的实验仪器装置图”的考查要求。
(7)要主动利用题中化学方程式信息、图表中的相对分子质量信息、题中有关实验数据,列式进行产率计算。
(8)要利用图表中异戊醇、乙酸异戊酯沸点信息分析实验误差后作答。
重视题给信息并主动迁移应用是解答此题的关键。
近年此类高考实验题密集出现,培养学生信息处理、加工和应用能力具有紧迫性和现实性。
三、熟练题型解法,训练规范作答
不同类型问题都有相应解题方法,熟练题型解法,训练规范作答才能高质量地解题。
例如:操作原理简答题一般要围绕实验目的,结合题给信息,从物质性质、仪器操作、反应原理、减少误差、产品保护等方面回答;检验题规范表述一般是:取样→操作→现象→结论(实验方案设计题可参照这个表述);实验评价题一般从实验方案的“科学性、安全性、可行性、简约性”这几个方面去回答;误差要从实验原理、操作过程、计算表达式等方面分析;计算题一般依据守恒(元素守恒、电子守恒、电荷守恒)列式计算或多步反应列关系式计算等,同时注意化学用语规范。
近年来高考实验题与工业流程题有了一些交叉,可借助工业流程题的解题思路进行相应训练。抓住“原料→产品”这一主线,“看懂箭头”,即密切注意进入反应体系物质与离开反应体系物质的状态和价态,再展开思考和分析,不失为此类实验题解题的好做法。
例3(2015年全国新课标Ⅱ卷28题)
二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问題:
(1)工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为___________________。
(2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2:
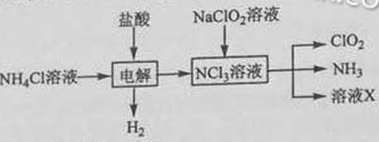

①电解时发生反应的化学方程式为___________________ 。
②溶液X中大量存在的阴离子有__________。
③除去ClO2中的NH3可选用的试剂是_______(填标号)。
a.水b.碱石灰c.浓硫酸d.饱和食盐水
(3)用下图装置可以测定混合气中ClO2的含量:
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入 3 mL稀硫酸:
Ⅱ.在玻璃液封装置中加入水.使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中:
Ⅴ.用0.1000 mol·L-1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-= 2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
2I-+S4O62-),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
①锥形瓶内ClO2与碘化钾反应的离子方程式为___________________。
②玻璃液封装置的作用是________________。
③V中加入的指示剂通常为____________,滴定至终点的现象是_________________。
④测得混合气中ClO2的质量为______________g。
(4)O2处理过的饮用水会含有一定量的亚氯酸盐。若要除去超标的亚氯酸盐,下列物质最适宜的是_______(填标号)。
a.明矾 b.碘化钾c.盐酸 d.硫酸亚铁
分析:本题对化学实验能力的考查全面完整,试题有流程题的一些特征。
(1)考查氧化还原反应原理,应用化合价升降法得出2:1。
- (2)可利用流程题解题思路,找出反应物和生成物,进行电解和制备的方程式配平:NH4Cl+2HCl
3H2↑+NCl3 ; 由6ClO2-+NCl3+3H2O=6ClO2+NH3+3Cl-+3OH-,可知溶液X中大量存在的阴离子有Cl—、OH— ;③由信息“ClO2易溶于水”和NH3的性质推知答案为c。
- 参考文献
(3)①应用离子方程式配平技巧得出:2ClO2+10I-+8H+=2Cl-+5I2+4H2O ,注意化学用语规范。
②此题考查仪器用途,也是考查ClO2测定原理,应利用题给信息“ClO2易溶于水”,从减小误差的角度思考,玻璃液封装置的作用是是吸收残余的二氧化氯气体(或避免碘的逸出)。
③V中加入的指示剂为淀粉溶液;“滴定至终点的现象”规范表述是“溶液由蓝色变为无色,且半分钟内溶液颜色不再改变”。
④计算题一般可用关系式法,此题可根据多步反应方程式列出关系式:2ClO2∽5I2∽10S2O32-计算;此题注意有效数字的规范,应保留四位有效数字:0.02700。
(4)考虑还原性和生成铁离子的净水作用选d。
此题涉及的问题类型较多,解法各异,熟练题型解法,注意规范作答就能顺利解题。
强化实验题解题策略指导和训练,使学生的学科素养和学科能力得到提高,才能在高考中取得较满意的成绩。
[1] 教育部考试中心. 2016年普通高等学校招生全国统一考试大纲(理科). 北京:高等教育出版社,2015
[2] 教育部考试中心. 2016年普通高等学校招生全国统一考试大纲的说明(理科). 北京:高等教育出版社,2015
|
|

